العلاج البيولوجي لمرض الصدفية عند الأطفال (الجزء الأول)
مقدمة لالصدفية عند الأطفال
الصدفية هي مرض جلدي التهابي مزمن متكرر تتوسطه الخلايا الليمفاوية التائية. ويرتبط بمضاعفات مختلفة، مما يؤثر بشدة على نوعية حياة المرضى ومقدمي الرعاية والأسر.
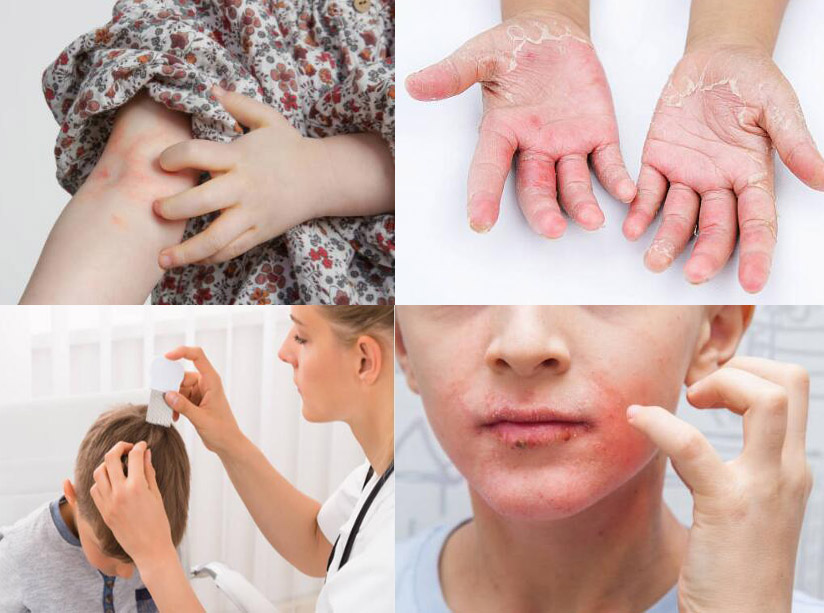
صدفيةيتميز بخلل التنظيم المناعي مما يؤدي إلى انتشار غير طبيعي للخلايا الكيراتينية الجلدية وتسلل الخلايا الالتهابية. سريريًا، يظهر المرض على شكل لويحات حمامية ذات حدود محددة ومغطاة بقشور فضية أو ميكاوية. في حين أن الصدفية يمكن أن تحدث في أي عمر، إلا أن ما يقرب من ثلث المرضى تظهر عليهم الأعراض أثناء الطفولة. بسبب الأبحاث الوبائية المحدودة على مجموعات الأطفال، فإن حدوث الصدفية عند الأطفال لا يزال غير واضح. في أوروبا، يتراوح معدل الانتشار من 0.17% إلى 1.5%، مع زيادة مطردة في معدل الإصابة مع تقدم العمر، حيث يبلغ ذروته عند سن 18 عامًا. تظهر الصدفية عند الأطفال على شكل لويحات حمامية متقشرة أصغر مع ارتشاح وتقشر أقل مقارنة بالبالغين.
تم إحراز تقدم كبير في توضيح الآلية المرضية المعقدة لمرض الصدفية، مما أدى إلى تطوير التجارب السريرية والموافقة على العلاجات المستهدفة لمرضى الأطفال.
تركز هذه المقالة، من خلال التحليل السردي للأدبيات الأكاديمية ذات الصلة، في المقام الأول على أحدث المفاهيم المتعلقة بإمراض الصدفية عند الأطفال والعلاج الدوائي الحالي. تم البحث في قواعد بيانات مجلات وGoogle مختص بمجال علمي وClinicaltrials.حكومة لتحديد الأبحاث المتعلقة بالصدفية لدى الأطفال.
الفيزيولوجيا المرضية للصدفية عند الأطفال
الصدفية مرض جلدي متعدد العوامل. يعتمد التسبب في المرض المناعي على التفاعل المعقد بين القابلية الوراثية والعوامل البيئية والمناعة الفطرية ومكونات المناعة التكيفية. ويتميز بالنمو المفرط والتمايز غير الطبيعي للخلايا الكيراتينية الجلدية، إلى جانب الالتهاب المستمر. ما يقرب من ثلث مرضى الصدفية لديهم أقارب من الدرجة الأولى مصابين بالمرض، مما يسلط الضوء على أهمية الوراثة. العوامل البيئية قد تساهم في تطور المرض. تشمل عوامل خطر الإصابة بالصدفية لدى البالغين التدخين، واستهلاك الكحول، والسمنة، والإجهاد، والالتهابات (خاصة التهاب البلعوم العقدي)، والصدمات الميكانيكية البسيطة. لم تتم دراسة تأثير عوامل نمط الحياة على الصدفية عند الأطفال على نطاق واسع، ولكن تم تحديد التهاب البلعوم العقدي أو التهاب الجلد العقدي حول الشرج، وارتفاع مؤشر كتلة الجسم (مؤشر كتلة الجسم)، والتعرض لدخان التبغ في المنزل كمحفزات محتملة.
يتم تحفيز الصدفية في المقام الأول عن طريق الخلية التائية المساعدة 17 (ث17) التي تنتج الإنترلوكين (انا) -17، والذي يعتبر من السيتوكينات الرئيسية التي تؤثر على تكوين اللويحة الصدفية. تعمل السيتوكينات المؤثرة انا-17 (انا-17A وIL-17C وIL-17F) على الخلايا الكيراتينية والخلايا البطانية والخلايا المناعية، مما يعزز تضخم البشرة في الصدفية اللويحية والمسارات المؤيدة للالتهابات. يلعب انترلوكين 23 (انا-23) دورًا حاسمًا في بقاء خلايا ث17 المسببة للأمراض وتوسيعها. يظهر المرضى الصغار مستويات أعلى بكثير من انا-17 و انا-22 مقارنة بالأطفال الأصحاء ومرضى الصدفية البالغين. ومع ذلك، فإن مستويات عامل نخر الورم (تنف) والخلايا التائية المنتجة لـ انا-22 أعلى في الجلد المصاب مقارنة بالبالغين، في حين أن مستويات الخلايا التائية المنتجة لـ انا-17 أقل بشكل ملحوظ.
علاج الصدفية اللويحية المزمنة الشديدة عند الأطفال
يتطلب اتخاذ القرار بشأن متى وكيف يبدأ العلاج الجهازي المناسب لمرض الصدفية عند الأطفال دراسة متأنية وشاملة تتضمن عوامل متعددة، وفي المقام الأول شدة الصدفية. يعد تقييم الخطورة أمرًا بالغ الأهمية لتوجيه قرارات العلاج، وذلك باستخدام المعلمات الموضوعية والذاتية، بما في ذلك منطقة الصدفية ومؤشر الخطورة (باسي)، ومساحة سطح الجسم (جيش صرب البوسنة)، ومؤشر جودة الحياة للأمراض الجلدية للأطفال (CDLQI).
يمكن تصنيف الصدفية عند الأطفال إلى خفيفة ومعتدلة/شديدة أو خفيفة ومعتدلة وشديدة. المرضى الذين يعانون من الصدفية الشديدة، كمرشحين للعلاج الجهازي و/أوالعلاج بالضوء، يجب أن يستوفي واحدًا على الأقل من المعايير التالية: باسي ≥ 10، جيش صرب البوسنة ≥ 10، CDLQI ≥ 10. إشراك المناطق التي يصعب علاجها مثل الوجه والكفين والأخمصين والأعضاء التناسلية والأظافر، أو فشل العلاج الموضعي ، يصنف على أنه شديد بغض النظر عن شدة المرض.
الأدوية التقليدية
لم تتم الموافقة على طرق العلاج التقليدية المضادة للصدفية مثل الميثوتريكسيت والسيكلوسبورين والأسيتريتين لعلاج مرضى الصدفية الشديدة لدى الأطفال. ومع ذلك، فقد تم استخدام هذه الأدوية بشكل متكرر في الماضي، وإن كان ذلك كعلاجات خارج نطاق التسمية. غالبًا ما تتضمن دراسات العالم الحقيقي سلسلة حالات بأثر رجعي تبحث في فعالية وسلامة الميثوتريكسيت والسيكلوسبورين والأسيتريتين. نظرًا لوجود أدوية أخرى معتمدة متاحة لعلاج الصدفية عند الأطفال، فلا ينبغي اعتبار العلاجات التقليدية من عوامل الخط الأول. ومع ذلك، يمكن استخدام الأدوية التقليدية مع الأدوية البيولوجية، خاصة في الحالات المقاومة أو المرضى الذين يعانون من فقدان ثانوي للفعالية. من المرجح أن يتلقى مرضى الصدفية الراحية الأخمصية علاجًا جهازيًا مشتركًا وعلاجًا بيولوجيًا مقارنة بالأطفال الذين يعانون من الصدفية اللويحية المعممة.
العلاجات البيولوجية
أحدثت العلاجات البيولوجية، التي تتميز بفعالية عالية، ومخاوف قليلة تتعلق بالسلامة، ثورة في نهج علاج الصدفية اللويحية المتوسطة إلى الشديدة في مرحلة الطفولة. وتشمل مزايا البيولوجيا فعالية عالية، ومتطلبات مراقبة مختبرية أقل. بالإضافة إلى ذلك، لا يرتبط العلاج طويل الأمد بسمية الأعضاء.
حاليًا، هناك ثلاث فئات من الأدوية البيولوجية لعلاج الصدفية عند الأطفال: مثبطات تنف-α، والأجسام المضادة لـ إيل12/23، والأجسام المضادة وحيدة النسيلة المضادة لـ إيل17. إيتانرسيبت، وadalimumab، وustekinumab، وsecukinumab، وixekizumab هي خمسة مستحضرات بيولوجية معتمدة في أوروبا لعلاج الصدفية عند الأطفال، في حين أن أداليموماب لم تتم الموافقة عليه بعد من قبل إدارة الغذاء والدواء.
يجب أن تدار جميع الأدوية البيولوجية المعتمدة لعلاج الصدفية عند الأطفال تحت الجلد. ويقدم الجدول 1 الجرعات الموصى بها.
قبل البدء في العلاج، من الضروري إجراء فحص مناسب مماثل لتلك التي يتم إجراؤها لدى البالغين. قبل البدء في العلاج البيولوجي، من الضروري ضمان التطعيم في الوقت المناسب وإعطاء أي لقاحات ضرورية. يعد تحديد ما إذا كان المريض قد أصيب بالجدري المائي أو تلقى التطعيم أمرًا بالغ الأهمية أيضًا.
مثبطات TNFα
تم استخدام مثبطات TNFα لأكثر من عقدين من الزمن في علاج التهاب المفاصل الروماتويدي، والتهاب المفاصل الشبابي مجهول السبب، والتهاب القولون التقرحي، ومرض كرون عند الأطفال. يُوصف أداليموماب، باعتباره جسمًا مضادًا بشريًا وحيد النسيلة، لعلاج أمراض مختلفة. كان إيتانرسيبت أول دواء بيولوجي تمت الموافقة عليه لعلاج الصدفية عند الأطفال. وفي وقت لاحق، تمت الموافقة على أداليموماب من قبل وكالة الأدوية الأوروبية لعلاج الصدفية الشديدة لدى الأطفال. بعد انتهاء صلاحية براءة الاختراع، تمت الموافقة على البدائل الحيوية المتعددة لـ etanercept و أداليموماب من قبل وكالة الأدوية الأوروبية. نظرًا للاختلافات البسيطة في التكلفة، يتم استخدامها بشكل أساسي في الدول الأوروبية.
إيتانرسيبت
إيتانرسيبت، وهو بروتين مؤتلف، هو بروتين مستقبل تنف-α قابل للذوبان يمنع ارتباط تنف-α بمستقبله. بالر وآخرون. أكدت فعالية وسلامة عقار إيتانرسيبت مقارنة بالعلاج الوهمي في تجربة سريرية عشوائية شملت 211 مريضًا تتراوح أعمارهم بين 4 و17 عامًا مصابين بالصدفية. على مدار 12 أسبوعًا من العلاج، حقق 57% من المرضى الذين يتلقون عقار إيتانرسيبت (بجرعة 0.8 مجم/كجم، حتى 50 مجم) باسي 75 (P &لتر;0.001)، بينما وصل 11% فقط من المرضى الذين عولجوا بالعلاج الوهمي إلى باسي 75 (P &لتر;0.001). &لتر;0.001). حقق المرضى الذين عولجوا باستخدام إيتانرسيبت معدلات أعلى لاستجابة باسي 50 (75% مقابل 23%)، واستجابة باسي 90 (27% مقابل 7%)، وحالة واضحة أو شبه واضحة وفقًا للتقييم العالمي للأطباء (بي جي ايه) (53 مقابل 7%). 13%) مقارنة بالمجموعة الثانية (P &لتر;0.001). أظهرت دراسة تمديد مفتوحة لمدة 5 سنوات سلامة العلاج بالإيتانيرسيبت وفعاليته المستدامة على المدى الطويل دون آثار جانبية غير متوقعة. وأظهرت تجارب عشوائية أخرى تأثيرات هامة سريريًا على أمراض محددة ونوعية الحياة بشكل عام. تؤكد البيانات الواقعية فعالية وسلامة عقار إيتانيرسيبت لدى مرضى الأطفال الذين يعانون من الصدفية اللويحية المتوسطة إلى الشديدة.
في أوروبا، تمت الموافقة على إيتانيرسيبت لعلاج الأطفال الذين تبلغ أعمارهم 6 سنوات فما فوق والذين لا يتحملون العلاجات الجهازية الأخرى أوالعلاج بالضوء,ومن ثم فهو يعتبر علاج الخط الثاني. في الولايات المتحدة، تمت الموافقة عليه لعلاج الصدفية اللويحية المزمنة المعتدلة إلى الشديدة لدى الأطفال الذين تتراوح أعمارهم بين 4 سنوات وما فوق.
أداليموماب
أظهر أداليموماب، وهو جسم مضاد أحادي النسيلة من الغلوبولين المناعي البشري المؤتلف بالكامل G1، نتائج واعدة في تجربة سريرية عشوائية للأطفال والمراهقين المصابين بالصدفية الذين يتلقون علاج أداليموماب أو ميثوتريكسات. حقق المرضى الذين عولجوا بالجرعة القياسية (0.8 ملغم/كغم) من أداليموماب باسي 75 بمعدل 57.9% بعد 16 أسبوعًا من العلاج، مقارنة بـ 32% فقط من المرضى الذين يتلقون الميثوتريكسيت. كانت نقطة نهاية الفعالية الثانوية لاستجابة باسي 90 مع علاج أداليموماب (29% مقابل 22%، p = 0.466) متفوقة أيضًا على مجموعة الميثوتريكسيت عن طريق الفم ولكنها لم تصل إلى دلالة إحصائية. في دراسة طويلة الأمد قيمت 108 أطفال على مدى 52 أسبوعًا، ظلت فعالية أداليموماب ثابتة أو تحسنت بمرور الوقت دون أي إشارات أمان جديدة.